
近年来,细胞治疗的“明星”——CAR-T,不再仅仅属于血液肿瘤科。研究者发现:针对致病 B 细胞的精准清除,有望从根源上改变一些顽固性自身免疫病的自然史。
CAR-T(嵌合抗原受体 T 细胞)通过把患者或供者的 T 细胞基因改造,使其识别并杀死表达特定靶点(最常见的是 CD19)的细胞。
在许多自身免疫病——例如系统性红斑狼疮(SLE)、硬皮病、重症肌无力等——异常 B 细胞或产生自身抗体的浆细胞是致病核心。把这些病理性 B 细胞“清零”后,免疫系统有机会重建,炎症与器官损伤可以得到显著缓解,甚至达到长期无药缓解。
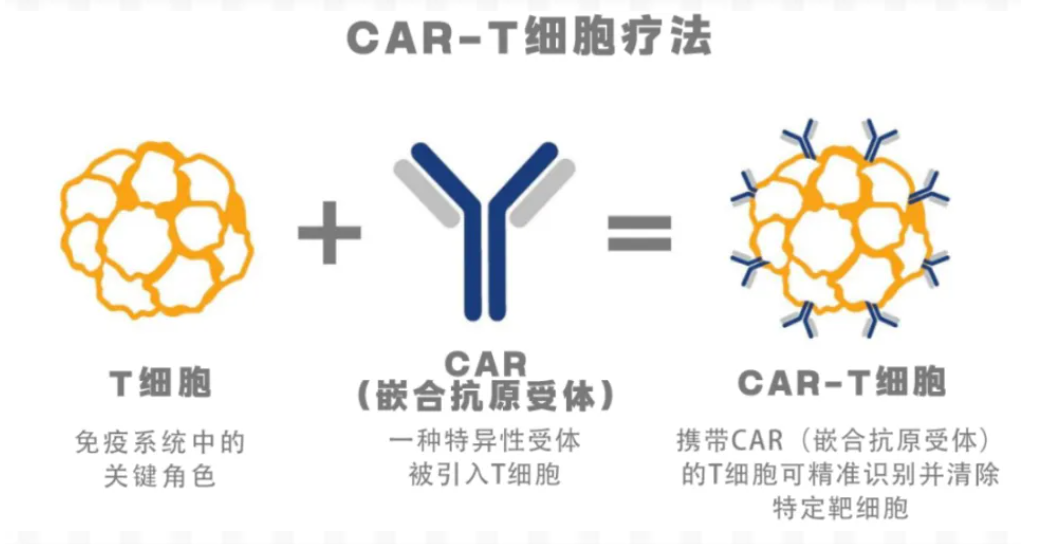
这个“从源头治理”的思路,是 CAR-T 从抗癌跨界到风湿免疫学的生物学基础。
现在用于自身免疫病的 CAR-T 研究,主要分为三条技术路径:
1.自体 CD19-CAR-T(传统体外改造):取患者 T 细胞体外改造再回输,是目前证据最多的方式。
代表性报道显示:若干难治性 SLE 病例在接受抗-CD19 CAR-T 后,于数月内进入深度缓解,并能维持较长时间的无药状态,且大多数患者仅出现轻-中度的细胞因子释放综合征(CRS)。这些早期临床/病例系列为 CAR-T 在自身免疫病的可行性提供了有力证据。
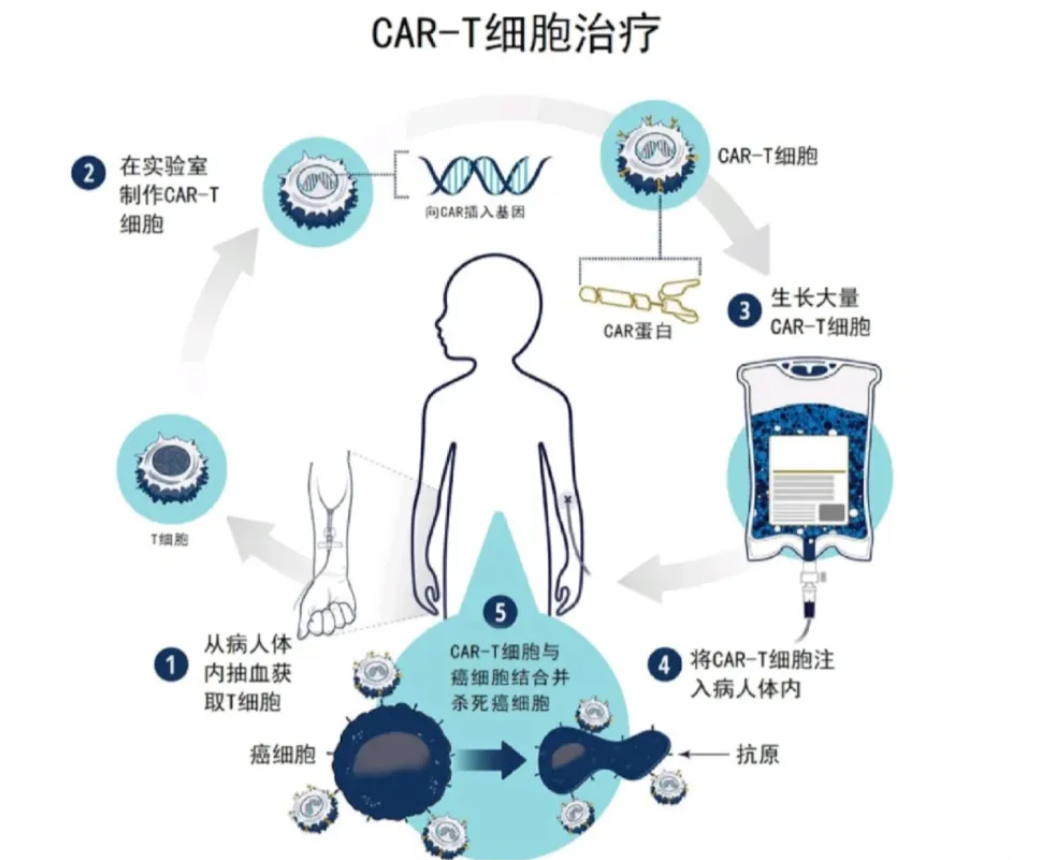
2.全成体(off-the-shelf)/同种异体 CAR-T:为解决自体制备耗时、成本高的问题,研究者开发供体来源的“现成”CAR-T。
近期小规模研究与报道显示,全成体 CD19-CAR-T 在部分难治自身免疫病中也能诱导缓解,并支持更快的可及性,但需关注移植物-抗-宿主(GvHD)或排斥等特有风险。相关多中心探索正在推进。
3.体内工程(in-vivo)与 LNP/mRNA 递送:最具颠覆性的是利用脂质纳米颗粒(LNP)携带 mRNA,直接在体内让 T 细胞表达 CAR,省去抽血、体外培养流程。
这类技术在动物与早期临床探索中显示能快速生成功能性 CAR-T,未来有望显著降低成本并扩大适用人群。该方向在 2024–2025 年迅速进入临床关注清单。
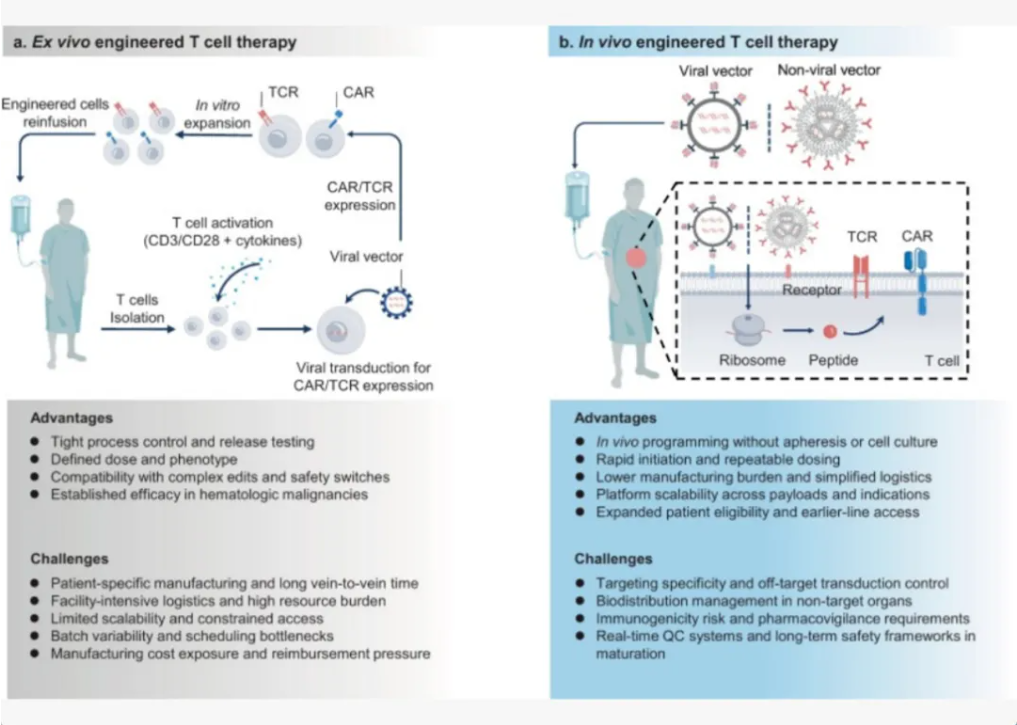
此外,还有 CAR-NK、复合靶点(如 BCMA+CD19 复合 CAR)等策略,为不同病理类型提供靶点选择与安全性调控的可能性。总体来看,从个例到小队列,再到早期多中心试验,证据在逐步积累,但仍以早期研究为主。
三、最新临床数据:疗效显著,安全性可控💡
2024-2025年多项国际顶刊研究证实,CAR-T疗法在自身免疫病治疗中展现出颠覆性潜力。
在难治性系统性红斑狼疮(SLE) 领域:
美国诺华的CD19 CAR-T疗法Ⅱ期试验中,62%的患者实现12个月以上持续缓解且无需激素。
我国瑞金医院团队的自体CD19 CAR-T研究,对15例重度狼疮患者中位随访10个月,完全缓解率达53%,且仅2例出现轻度细胞因子释放综合征(CRS),无严重不良事件。
在类风湿关节炎、干燥综合征等领域,CD20、BCMA CAR-T的早期临床数据同样积极。
值得关注的是,治疗后患者免疫功能可逐步重建,长期随访未发现明显远期毒性,为实现“功能性治愈”提供了可能。目前,全球已有12款针对自免病的CAR-T疗法进入Ⅱ/Ⅲ期临床,预计2026年后将有首款药物获批上市。
除了这些外,风湿免疫性患者(类风湿性关节炎,强直,皮肌炎,红斑狼疮,结肠炎,血小板减少等等)也可以尝试申请创新药,入组成功后,可安排就近的三甲医院免费用药,点击免费申请用药即可报名
这一从抗癌到攻克自免病的跨界突破,是精准医疗的延伸。未来随着“一药多靶”“现货可及”等技术迭代,有望为千万患者带来全新希望。

咨询热线:15313289818
工作日 9:00-18:00



